Determination of Compound-Specific Carbon Isotopic Compositions of Trace-Level Volatile Organic Compounds in Aqueous Phases Using SPME-Cryofocus GC-IRMS Technique
-
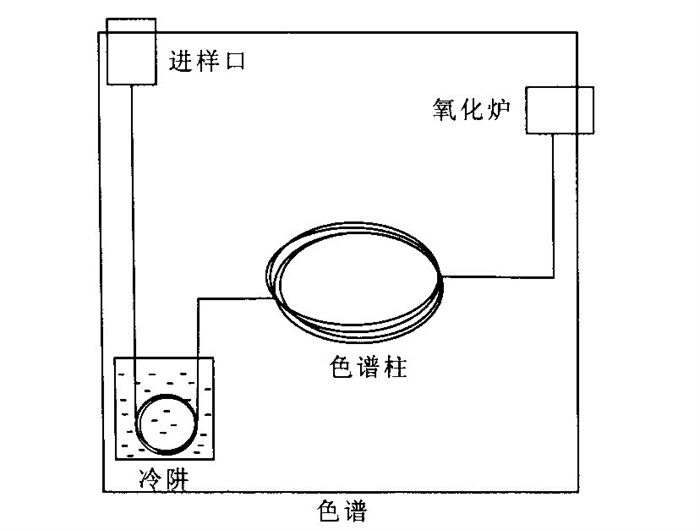
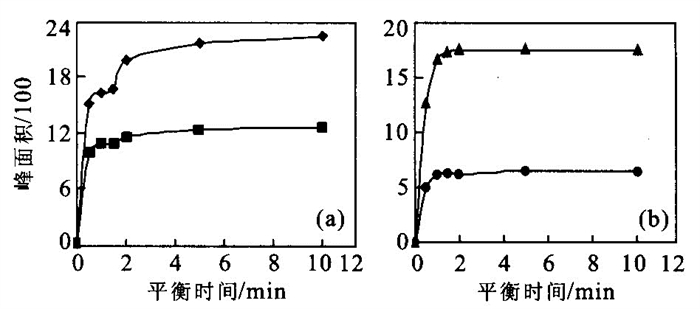
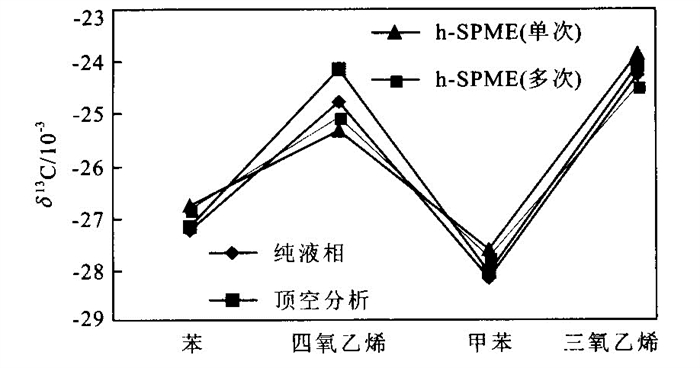
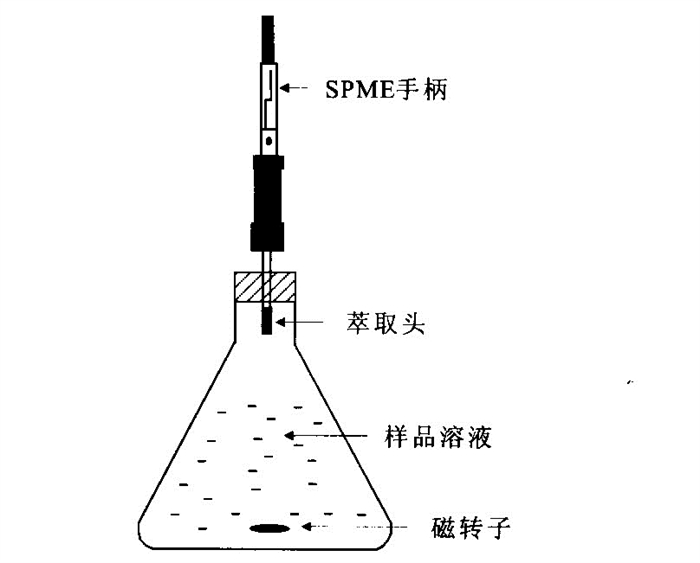
摘要: 单体碳同位素分析是进行污染物来源判识与过程示踪的有力工具, 然而有机污染物浓度低、难以萃取富集, 极大地限制了该技术的广泛应用.采用固相微萃取-冷阱富集GC-IRMS技术对水中痕量挥发性有机物进行了单体碳稳定同位素分析, 样品经SPME萃取富集后在色谱进样口冷冻成形, 样品多次进样得以累积从而满足了检测限的要求.本方法检出限较目前文献所报道的SPME方法提高了1个数量级.在优化的条件下, 对低浓度的三氯乙烯、四氯乙烯、苯以及甲苯的水溶液进行了单体碳同位素组成测定, 测定结果与纯液相中的同位素值相比, 同位素分析误差不超过0.5×10-3, 而分析的精度达到±0.3×10-3.固相微萃取-冷阱富集可以提供高效准确的单体碳同位素分析, 该方法适用于水体中痕量挥发性有机污染物的同位素组成测定.Abstract: Compound-specific carbon isotope ration analysis is a promising tool to assess the origin and fate of organic contaminants, however, the low concentrations of dissolved organic pollutants and the difficulty to concentrate or extract have been the major facts limiting the application of stable isotope tracing techniques at contaminated field sites. In this paper, we developed a method combining SPME with cryofocus technique for the compound-specific carbon isotope analysis of volatile organic compounds in aqueous phase, samples were extracted with SPME and then cryofocus to the front part of GC column, the samples were cumulated after several times of extraction and meet the detection limit. The detection limit using this method was 10 times improved than the conventional SPME method. Under the optimum analytical condition, aqueous samples Trichloroethene, Tetrachloroethene, Benzene and Toluene were analyzed, δ13C fractionation compared to pure-phase analysis was less than 0.5×10-3, the reproducibility was better than ±0.3×10-3. GC-IRMS coupling with SPME and Cryofocus technique proved to be a promising and accurate method for the determination of carbon isotope composition of trace-level volatile organic compounds in aqueous phases.
-
表 1 采用固相微萃取技术测定碳同位素与文献结果比较
Table 1. Comparison of detection limit for carbon isotope analysis using SPME with references

-
Authur, C., Pawliszyn, J., 1990. Solid-phase microextraction with thermal desorption using fused silica optical fibers. Anal. Chem., 62: 2145-2148. doi: 10.1021/ac00218a019 Beneteau, K.M., Arave, R., Frape, S.K., 1999. Isotopic characterization of chlorinated solvent-laboratory and field results. Org. Geochem., 30: 739-753. doi: 10.1016/S0146-6380(99)00057-1 Dias, R.F., Freeman, K.H., 1997. Carbon isotope analysis of semivolatile organic compounds in aqueous media using solid-phase microextraction and isotope ration monitorning GC/MS. Anal. Chem., 69: 944-950. doi: 10.1021/ac960635+ Harris, S.A., Whiticar, M.J., Eek, M.K., 1999. Molecular and isotopic analysis of oils by solid phase microextraction of gasoline range hydrocarbons. Org. Geochem., 30: 721-737. doi: 10.1016/S0146-6380(99)00056-X Huang, L., Sturchio, N.C., Abrajano, T., et al., 1999. Carbon and chlorine isotope fractionation of chlorinated aliphatic hydrocarbons by evaporation. Org. Geochem., 30: 777-785. doi: 10.1016/S0146-6380(99)00060-1 Hunkeler, D., Aravena, R., 2000. Determination of compound-specific carbon isotope ratios of chlorinated methanes, ethenes, and ethenes in aqueous samples. Environ. Sci. Technol., 34: 2839-2844. doi: 10.1021/es991178s Menéndez, J.C.F., Sánchez, M.L.F., Uría, J.E.S., et al., 2000. Static headspace, solid-phase microextraction and headspace solid-phase microextraction for BTEX determination in aqueous samples by gas chromatography. Anal. Chim. Acta, 415: 9-20. doi: 10.1016/S0003-2670(00)00862-X Poulson, S.R., Drever, J.I., 1999. Stable isotope(C, Cl and H)fractionation during vaporization of trichloroethylene. Environ. Sci. Technol., 33: 3689-3694. doi: 10.1021/es990406f Slater, G.F., Dempster, H.S., Lollar, B.S., et al., 1999. Headspace analysis: A new application for isotopic characterization of dissolved organic contaminants. Environ. Sci. Technol., 33: 190-194. doi: 10.1021/es9803254 Yang, J., Tsai, S.S., 2001. Development of headspace solid-phase microextraction/attenuated total reflection infrared chemical sensing method for the determination of volatile organic compounds in aqueous solution. Anal. Chim. Acta, 436: 31-40. doi: 10.1016/S0003-2670(01)00890-X Zhang, Z., Yang, M., Pawliszyn, J., 1994. Solid-phase microextraction. Anal. Chem., 66: 844-853. -








 下载:
下载: